คู่กรด-เบส
คู่กรด – เบส
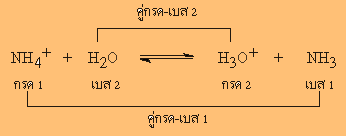
คู่กรด – เบส คือ สารที่เป็นคู่กรด-เบสกัน H + ต่างกัน 1 ตัว โดยที่ คู่กรดจะมี H + มากกว่าคู่เบส 1 ตัว
ความแรงของกรดและเบส = การแตกตัวในการให้โปรตอน(กรด) ความสามารถในการรับโปรตอน(เบส)
CH 3COOH (aq) + H 2O (aq) CH 3COO - (aq) + H 3O + (aq)
<<< เราต้องรู้ทิศทางการเลื่อนของสมดุลก่อน เราจึงจะบอกถึงความแรงได้>>>
1. ถ้าสมดุลเลื่อนไปทางขวา CH 3COOH เป็นกรดแรงกว่า H 3O + / H 2O เป็นเบสแรงกว่า CH 3COO -
2. ถ้าสมดุลเลื่อนไปทางซ้าย H 3O + เป็นกรดแรงกว่า CH 3COOH / CH 3COO - เป็นเบสแรงกว่า H 2O
ถ้าค่า K > 1 สมดุลเลื่อนไปข้างหน้า(สารผลิตภัณฑ์มากกว่าสารตั้งต้น)
K < 1 สมดุลเลื่อนย้อนกลับ(สารผลิตภัณฑ์น้อยกว่าสารตั้งต้น)
K = 1 ไปข้างหน้าเท่ากับย้อนกลับ (สารผลิตภัณฑ์=สารตั้งต้น) ความแรงทั้ง 2 ข้างเท่ากัน
เปรียบเทียบกรดแก่กับเบสแก่
กรดแก่
เบสแก่
1. กรดแก่มีอะไรบ้าง
2. กรด Hydro = HCl HBr HI
3. กรด Oxy = HNO3 HClO3 HClO4 H2SO4
4. การแตกตัว 100%
5. การเป็นอิเล็กโทรไลต์ = แก่
2 . เบสแก่มีอะไรบ้าง
2. หมู่ 1 = LiOH NaOH KOH RbOH CsOH
3. หมู่ 2 = Ca(OH)2 Sr(OH)2 Ba(OH)2
4. การแตกตัว 100 % ( หมู่ 2 แตก 200 %)
5. การเป็นอิเล็กโทรไลต์ = แก่
กรดแก่ ( strong acid) คือกรดที่สามารถแตกตัวได้ 100% ในน้ำ เช่น HCl H2SO4 HN03 HBr HClO4 และ HI
เบสแก่ ( weak base) คือกรดที่สามารถแตกตัวได้ 100% ในน้ำ เช่น Hydroxide ของธาตุหมู่ 1 และ 2 ( NaOH LiOH CsOH Ba(OH) 2 Ca(OH) 2 )
กรดอ่อน ( weak acid) คือกรดที่สามารถแตกตัวเป็นไอออนได้เพียงบางส่วน เช่น กรดอะซิติคในน้ำส้มสายชู (vinegar) ยาแอสไพริน (acetylsalicylic acid) ใช้บรรเทาอาการปวดศรีษะ saccharin เป็นสารเพิ่มความหวาน niacin (nicotinic acid) หรือ ไวตามินบี เป็นต้น ตัวอย่างปฏิกิริยาของสารละลายกรด CH 3COOH ในส่วนผสมของน้ำส้มสายชูจะมีดังนี้ :
CH 3COOH (aq) + H2O (1) H3O + (aq) + CH3COO - (aq) มีค่า K a
เบสอ่อน (weak base) คือเบสที่สามารถแตกตัวเป็นไออนได้เพียงบางส่วน เช่น NH 3 urea aniline เป็นต้น ตัวอย่างปฏิกิริยาของ ammonia มีดังนี้
NH3(aq) + H2O (aq) NH4 + (aq) + OH - (aq)

ที่มา http://www.bloggang.com/data/nooyingja/picture/1228329121.gif
*************************************************************
ทดสอบความเป็นกรด-เบสกับวัสดุหาง่ายยุค IMF
การรักษาสมดุลของกรด- เบสในมนุษย์







